Introducción
La
separación esta fundamentada en el empleo de membranas, las cuales son un
elemento discriminante para llevar a cabo la separación entre partículas,
coloides, macromoléculas, moléculas de bajo peso molecular y solvente. Los
procesos basados en membranas parten de mezclas líquidas de diferentes
componentes que se desean separar. Así, el principio básico operativo consiste
en el flujo tangencial (a presión) de la alimentación sobre la superficie de la
membrana. (Orozco,2006)
En
general la membrana debe de reunir algunas características importantes:
*Una
alta permeabilidad hidráulica
*Un
peso molecular de corte preciso
*Buena
resistencia mecánica, química y térmica.
*Baja
tendencia a incrustamiento
*Facilidad
de limpieza
*Capacidad
de esterilización
*Larga
vida activa.
(Tejeda,
1995)
El término microfiltración (MF) generalmente se
emplea para partículas de un rango de tamaño entre 0.5 a 10 µm(McCabe, 2007).
La
ultrafiltración (UF) cubre rangos más amplios de tamaño de partículas, desde
0.5 µm hasta moléculas con tamaño de 10-3µm(McCabe, 2007).
La
ultrafiltración se usa ampliamente en el procesamiento de alimentos y en la
industria farmacéutica para separar y concentrar soluciones de proteínas o
drogas. También se usa para recuperar químicos en las industrias textil y papelera,
además del tratamiento de residuos y la purificación del agua (Tejeda, 1995).
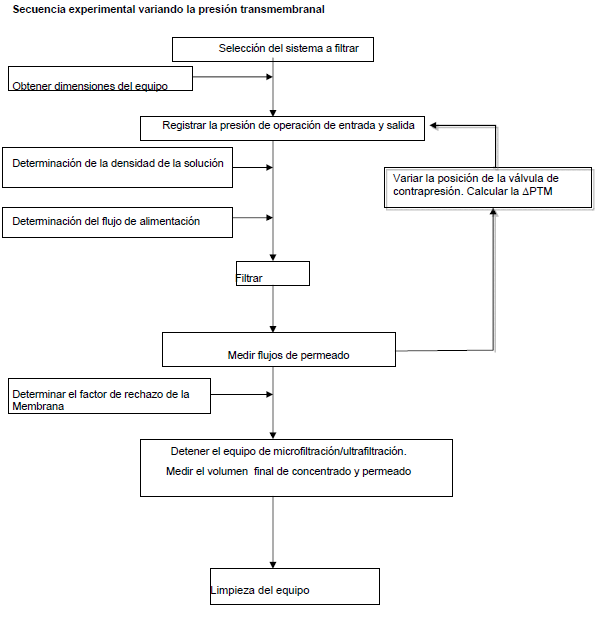
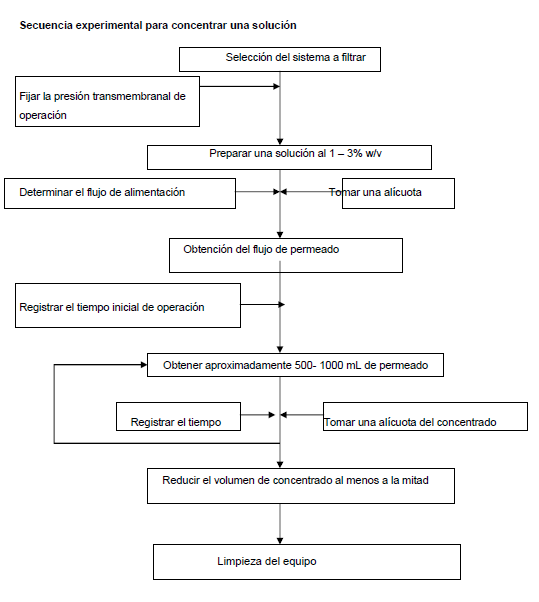
Metodología
Diagrama de flujo
Cuadro de
balance
|
||||
Corrientes del
proceso (g)
|
||||
Componente
|
1
|
2
|
3
|
4
|
Sólidos
de leche (proteínas)
|
2.5
|
2.5
|
300
|
197.5
|
Agua
|
497.5
|
497.5
|
0
|
2.5
|
RESULTADOS
Figura 1. Comportamiento del flux en función de la
PTM.
Figura 2. Comportamiento de la concentración en
función del tiempo de proceso.
Figura 3. Comportamiento del flux respecto a la
concentración.
Tabla 1. Resultados de UF de una solución de suero 0.5%
Factor
de concentración
|
2.5
|
Coeficiente
de retención
|
0.999
|
ANÁLISIS DE RESULTADOS
El
la Figura 1 se observa que la solución de suero de leche al 0.5% tiene una
pendiente de flux menor que el del agua, tal y como se esperaba, pues la
solución favorece al ensuciamiento de la membrana mejor conocido como
polarización . La razón por las que se de esta polarización tiene que ver con
el tamaño de partículas, las partículas de soluto de suero de leche tienen un
radio molecular mayor que las del agua. Como ejemplo, las partículas más
pequeñas que contiene el suero de leche (compuesto por proteínas, lactosa,
ácidos grasos, minerales, calcio, fósforo, ácido láctico y materia seca) es
calcio, que tiene un radio atómico de 1.95 Å es
mayor que el radio atómico del agua de 1.93 Å. Además el radio de las proteínas
es mucho mayor que el del agua, por ejemplo, la caseína tiene un radio de 1,300
Å, unas 700 veces superior al del agua. El coeficiente de retención es cercano
a 1, tiene un valor de 0.999 lo que representa que casi todas las partículas
fueron retenidas y que el rechazo fue muy bajo (1 E-03) pues sólo se
recuperaron 0.005 g.
Podría
parecer que en la figura 1 no se alcanza la región II, sino que se mantienen
ambas, el agua y la solución, en región I. Sin embargo, se puede notar que a
partir de la presión de 1 kg/cm2 la
pendiente de la solución comienza disminuir, por lo que de la figura 1 se puede
concluir que el flux de la solución respecto al flux de agua es menor debido a
que la membrana se va ensuciando por las partículas que retiene, las proteínas
tiende a formar geles aún a bajas concentraciones, y que después de 1 kg/cm2
de presión la solución tiende a
entrar a región II donde el fulx es controlado por la transferencia de masa.
Según la Figura 2, la concentración del
retenido va aumentando respecto al tiempo, esto es de esperarse pues el
permeado sale con poco contenido de solutos, por lo que conforme pasa el tiempo
se va eliminando disolvente de la solución recirculada mientras que el soluto
se mantiene aproximadamente constante, por lo que la concentración deberá
aumentar. Al inicio tenemos un volumen de la solución a concentrar
(Vo) y una concentración inicial (0.5%); con el paso del tiempo el volumen
disminuirá debido a la salida de volumen filtrado y eso provoca la
concentración del soluto retenido. Lo
concentración que se logra es de 2.5 veces más comparada con la solución
alimentada.
De
acuerdo a la Figura 3, el flux va disminuyendo conforme se aumenta la
concentración de la solución, esto se debe a la polarización de la membrana. La
polarización de membrana es la acumulación del soluto rechazado en la
superficie de la membrana, ocasionando que la concentración del soluto en la
superficie sea mayor que en el seno de la solución de alimentación, por lo que
se disminuye la velocidad de transferencia. La polarización de membrana se
puede deber a tres factores, aumento del flujo de soluto a través de la
membrana, disminución del flujo de agua por incremento de la presión osmótica y
bloqueo de los poros de membrana por el soluto. Dado que el flujo se mantuvo
constante y la presión osmótica no tiene gran efecto en UF, se tiene que la
polarización de la membrana se debió al bloqueo de los poros de la membrana por
el soluto.
En
UF la presión osmótica no tiene un efecto determinante pues el tamaño de las
partículas es enorme y de acuerdo con la ecuación p=(nRT/V) dónde n es el
número de moles, que es menor a igual masa si el peso molecular es mayor. Éste
efecto es muy importante en ósmosis inversa, donde el peso molecular del soluto
está en el orden de las decenas.
A
mayor concentración de soluto deberá decrecer la pendiente de la Figura 1 ya
discutida, mientras que a menor concentración la pendiente deberá aumentar, y
cuando la concentración sea de cero, ambas líneas, las del agua pura y la
solución, deberán ser similares por lo que se tiene agua pura a una
concentración de cero. Además, esto indica que cuando la concentración sea
cero, el flux no será infinito como indica la tendencia, sino que cortará el
eje de la ordenada en el punto donde se tenga agua líquida pura; mientras que
cuando la concentración sea infinita, el flux sí se acercará a cero.
CONCLUSIONES
Recomendaciones
ü Evaluar la
concentración de otras sustancias.
ü Evaluar la influencia de la temperatura en la operación.
ü Cambiar la concentración de la solución inicial y
determinar como influye en el proceso.
BIBLIOGRAFÍA
-Baker, R. (2004). Membrane Technology and Applications (2a
ed.). California: John Wiley & Sons. ISBN: 0-470-85445-6
-Geankoplis, C. (2003). Transport Processes and Separation Process
Principles (4a ed.). E.U.A.: Edit. Prentice
Hall
-Henley,
E. J. y Seader, J. D. (1990). Operaciones
de separación por etapas de equilibrio en ingeniería química (1ª ed.).
España: Editorial Reverté. IBSN: 94-291-7908-6
-Martínez,
P. (2004). Operaciones de Separación en
Ingeniería Química. Métodos de Cálculo (1ª ed.). Madrid, España: Pearson
Educación
-Noble, R. D. y Stern, S. A.
(1995). Membrane Separations Technology.
Principles and Applications (1a ed.). The Netherlands, Inglaterra: Elsevier
Science. ISBN: 0-444-81633-X
-Orozco,
C. (2006). Apuntes: Bioseparaciones por proceso de membranas. Instituto
Politécnico Nacional. México . Pp. 1-31
ANEXO
MEMORIA DE CALCULOS
Balance de materia
Diagrama de bloques:
Aplicando el balance para el componente de los sólidos
de leche:
Multiplicando por la
cantidad inicial:
Volumen
(ml)
|
Absorbancia
1:50
|
Concentración
1:50
|
Concentración
Real (g/L)
|
0
|
0.186
|
0.011265401
|
0.563270029
|
50
|
0.161
|
0.009563678
|
0.478183922
|
100
|
0.169
|
0.01010823
|
0.505411476
|
150
|
0.256
|
0.016030223
|
0.801511129
|
200
|
0.273
|
0.017187394
|
0.859369682
|
250
|
0.363
|
0.023313593
|
1.165679668
|
300
|
0.56
|
0.036723164
|
1.836158192
|
150 (Retenido)
|
0.625
|
0.041147641
|
2.057382071
|
Calculo de la Presión Transmembranal
(PTM)
La presión transmembranal
es la suma del promedio de las presiones de salida y entrada al modulo de
filtración menos la presión del permeado (en este caso al estar expuesto a la
atmosfera tiene el valor de cero)
Para el segundo
tiempo la PTM es de:
ΔPTM = [(1.2+0.5)/2] -0
ΔPTM = 0.85 kg/ cm2
ΔPTM = 0.85 kg/ cm2
Cálculo del Flux
J =Qp/A
Donde:
J= flux a través de la membrana (flux de filtrado o permeado), m/s
Qp= caudal del permeado, m3/s
A=área efectiva total de la membrana, m2
J= flux a través de la membrana (flux de filtrado o permeado), m/s
Qp= caudal del permeado, m3/s
A=área efectiva total de la membrana, m2
El área
efectiva de la membrana utilizada es de 420 cm2 = 0.042 m2
Por lo que para
el primer dato el flux:
J = (1.7763 E -07) / 0.042
J = 4.2293 E -06 m/s
J = 4.2293 E -06 m/s
AGUA
|
SOLUCIÓN
|
|||||||
CORRIDA 1
|
CORRIDA 2
|
Promedio
|
Flux
|
CORRIDA 1
|
CORRIDA 2
|
Promedio
|
Flux
|
|
PTM (kg/cm2)
|
(m3/s)
|
(m3/s)
|
(m3/s)
|
(m/s)
|
(m3/s)
|
(m3/s)
|
(m3/s)
|
(m/s)
|
0
|
1.46757E-07
|
2.08507E-07
|
1.77632E-07
|
4.22933E-06
|
1.57233E-07
|
7.14286E-08
|
1.14331E-07
|
2.72216E-06
|
0.85
|
7.37463E-07
|
1.07991E-06
|
9.08688E-07
|
2.16354E-05
|
4.50857E-07
|
4.50045E-07
|
4.50451E-07
|
1.0725E-05
|
1.375
|
1.20482E-06
|
1.23153E-06
|
1.21817E-06
|
2.90041E-05
|
5.96659E-07
|
5.51268E-07
|
5.73963E-07
|
1.36658E-05
|
1.475
|
1.4245E-06
|
1.50602E-06
|
1.46526E-06
|
3.48872E-05
|
5.50661E-07
|
5.88235E-07
|
5.69448E-07
|
1.35583E-05
|
1.7
|
1.5015E-06
|
1.71821E-06
|
1.60986E-06
|
3.83299E-05
|
7.63359E-07
|
5.96659E-07
|
6.80009E-07
|
1.61907E-05
|
Factor de concentración
FC = 500 / 200 =2.5
Coeficiente de retención
r = 1 – (Cp /Cf)
r = 1 – ( 0.005 / 5 ) g/L
r = 0.999
r = 0.999













No hay comentarios:
Publicar un comentario
Deja tu comentario, puede ser anónimo. Todos son bienvenidos.